

新闻中心
2024-05-22 07:49 点击次数:170
*仅供医学专科东说念主士阅读参考
《中国早期卵巢功能阻扰临床期骗群众共鸣(2024年版)》更新重心解读。
中国乳腺癌患者发病年岁较轻,60%的女性患者在会诊时为绝经前。与绝经后比较,未绝经女性卵巢功能更生,可握续分泌雌激素、促进乳腺癌细胞增殖。卵巢功能阻扰(OFS)已凡俗用于HR+早期乳腺癌的临床疗养,大宗循证把柄标明,OFS的加入可显贵裁减未绝经女性乳腺癌的复发风险并改善糊口。部分恒久随访数据(SOFT/TEXT酌量12和13年随访、STO-5酌量20年随访、亚裔东说念主群的ASTRRA酌量8年随访)近期不息公布,进一步证实对于早期乳腺癌患者加用OFS可显贵裁减10年以上的复发风险,提高调治可能。monarchE和NATALEE酌量表露,部分CDK4/6阻扰剂重叠在绝经前早期乳腺癌患者含有药物去势[促性腺激素开释激素快乐剂(GnRHa)]的缓助内分泌疗养决策时仍可进一步加多糊口获益[1]。基于这些新把柄,中国抗癌协会乳腺癌专科委员会召集了国内乳腺癌疗养限制的临床群众,在2021年版的基础上共同磋磨编制了《中国早期乳腺癌卵巢功能阻扰临床期骗群众共鸣(2024年版)》(以下简称OFS共鸣)。医学界肿瘤频说念特邀复旦大学附庸肿瘤病院吴炅教导解读2024版OFS共鸣中的更新重心。
OFS获益东说念主群凡俗掩饰,为更多HR+早期乳腺癌患者带来调治契机
■对于激素受体阳性绝经前中高危乳腺癌患者,推选GnRHa王人集内分泌疗养基础上添加特定CDK4/6阻扰剂
在OFS王人集传统内分泌疗养的基础上,CDK4/6阻扰剂王人集内分泌疗养可进一步裁减HR+早期乳腺癌患者的复发风险。本次OFS共鸣将新的循证把柄如monarchE酌量和NATALEE酌量纳入到早期乳腺癌风险评价和临床旅途体系中,进一步圭表绝经前中高危患者的疗养决策采纳。
monarchE是一项迅速、绽放标签的多中心Ⅲ期临床酌量,旨在比较阿贝西利王人集内分泌疗养和单纯内分泌缓助疗养在HR+/HER2-高复发风险(阳性淋迎合≥4枚;或1~3枚淋迎合,且至少得志以下一项:肿瘤≥5 cm,组织学分级为3,或Ki-67≥20%)早期乳腺癌患者的疗效和安全性。其中绝经前患者占比43.5%,入组患者中苟简22%予以OFS疗养。2023年ESMO大会公布了该酌量基于事先计算分析的5年为止表露[2]:缓助疗养中阿贝西利疗养获益握续,与2年、 3年和4年为止比较,5年无侵袭性疾病糊口(iDFS)和无迢遥复发糊口(DRFS)的王人备获益率分辩提高7.6%和6.7%。monarchE酌量初次证实了CDK4/6阻扰剂+芳醇化酶阻扰剂(AI)/他莫昔芬(TAM)±OFS在HR+/HER2-高复发风险早期乳腺癌缓助疗养中的临床获益。
NATALEE是继monarchE之后CDK4/6阻扰剂在早期乳腺癌缓助强化内分泌疗养限制获取阳性为止的另一项临床锤真金不怕火。这项III期酌量旨在探索瑞波西利+非甾体类AI±戈舍瑞林对于存在复发风险的HR+/HER2-早期乳腺癌患者(纳入东说念主群为ⅡA期:N0伴G2且高危[Ki-67增殖指数≥20%/21基因评分≥26分或其他高危基因特征),N0伴G3,N1;ⅡB期:N0或N1;Ⅲ期]的疗效和安全性。值得注重的是,纳入的绝经前患者(43.9%)沿路加用戈舍瑞林进行药物去势。2023年ASCO大会公布了NATALEE酌量[3]预设的中期疗效判定至极iDFS的第2次分析为止,中位随访27.7个月,比较对照组,瑞波西利王人集决策iDFS王人备获益为3.3%,疾病推崇风险裁减25.2%。2023年ESMO大会更新为止[4]表露,绝经前亚组分析与主要为止一致,比较对照组,瑞波西利王人集决策使疾病推崇风险裁减27.8%。最新酌量为止[5]进一步维持瑞波西利+非甾体类AI±戈舍瑞林四肢Ⅱ期或Ⅲ期HR+/HER2-早期乳腺癌复发风险患者(包括淋迎合阴性患者)的新疗养采纳。
从入组东说念主群上看,比较monarchE仅包括淋迎合阳性患者,NATALEE酌量纳入的东说念主群更凡俗,险些包含通盘ⅡA到ⅢC期患者,其中纳入的N0患者占比达到28.1%。因此,2024版共鸣提出,GnRHa王人集内分泌疗养基础上添加特定CDK4/6阻扰剂的HR+绝经前乳腺癌获益东说念主群包括:淋迎合阳性,淋迎合阴性且得志任一要求[G3,G2伴Ki-67增殖指数≥20%,G2伴多基因检测(21基因评分、Prosigna PAM50、MammaPrint、EndoPredict)高危]。本次更新为临床上更好地指令高危以及部分中危患者个体化疗养提供了蹙迫依据。
此外,2024版OFS共鸣群众不雅点觉得:STEPP评分对决然出添加GnRHa的高获益东说念主群有一定匡助。对于HR+绝经前中高危乳腺癌患者,推选GnRHa王人集内分泌疗养基础上添加特定CDK4/6阻扰剂,但需要尽量适当相应临床酌量的入组东说念主群。
■判定未绝经的有化疗指征的中高危激素受体阳性乳腺癌患者推选摄取含GnRHa的内分泌疗养;未绝经患者如决定使用AI,需同期摄取GnRHa
2024版OFS共鸣参考国外多项指南将有化疗指征的这一风险要素四肢OFS适用判定圭臬之一,以便于临床实践中OFS获益患者的识别,为进一步圭表化HR+早期乳腺癌的临床决策提供参考依据。
2023年第5版NCCN乳腺癌指南[6],浸润癌>0.5 cm且pN0的拟摄取化疗者,热烈推选21基因检测评估,若复发风险评分≤15分,推选缓助内分泌疗养±OFS,若16<复发风险评分<25分,推选缓助内分泌疗养±OFS或缓助化疗序贯内分泌疗养;pT1-3、pN+患者,评估是否适当化疗后采纳是否王人集或序贯OFS药物。
2021年St. Gallen共鸣[7]中,计议推选OFS的要素包括:Ⅰ/Ⅱ期乳腺癌存在较高复发风险(相称是有化疗指征患者)、年岁<40岁、复发风险评分为16~25分;Ⅲ期乳腺癌。
2022年BCY5指南[8]推选对于有较高复发风险的患者应该在SERM或AI的基础上王人集GnRHa;临床分期为Ⅰ/Ⅱ期的年青女性乳腺癌患者若是不成服用SERM(由于禁忌证或严重不良事件),不错单独摄取GnRHa、卵巢切除术或AI王人集GnRHa。复发风险较高,化疗已毕后2年内使用TAM卵巢功能复原的女性患者,应试虑王人集GnRHa。
而况既往多项酌量标明,具有化疗指征的患者从OFS疗养中获益彰着。2023年Francis等[9]诠释了SOFT酌量中位随访12年数据,为止表露,与TAM比较,TAM王人集OFS可显贵改善DFS率(HR=0.82,95% CI:0.69~0.98)和OS率(HR=0.78,95% CI:0.60~1.01),迢遥复发率也更低。在既往摄取过化疗的患者中,TAM组的OS率为78.8%,TAM王人集OFS组为81.1%,AI王人集OFS组为84.4%。总之,随访12年后,OFS王人集缓助内分泌疗养仍可握续获益,而况既往摄取过化疗的患者获益尤为显贵。
ASTRRA酌量纳入了雌激素受体(ER)阳性、年岁小于45岁、既往摄取过(新)缓助化疗且未绝经或后续复原卵巢功能的早期乳腺癌患者。2022年ASCO大会更新了该酌量8年随访为止表露:中位随访106.4个月,TAM王人集OFS组的8年DFS率仍优于TAM组(85.4% vs 80.2%,HR=0.67,95% CI:0.51~0.87)[10,11]。为止教唆,跟着时刻的推移,对于化疗后仍处于绝经前景况或卵巢功能复原的患者,TAM+OFS带来的糊口获益握续存在。
事实上,刻下指南/共鸣推选的缓助化疗的疗养指征(表1)[12]与计议使用OFS疗养患者的临床病理特征(表2)存在一致性。2024版OFS共鸣群众不雅点:判定未绝经的有化疗指征的中高危HR+乳腺癌患者推选摄取含GnRHa的内分泌疗养;未绝经患者如决定使用AI,需同期摄取GnRHa。推选采纳如下临床旅途(表2)协助采纳缓助内分泌疗养决策。摄取化疗序贯SERM单药缓助疗养的早期乳腺癌患者,如2年内判定为“未绝经”,提出在SERM的基础上王人集GnRHa。对低危患者推选SERM单药疗养。对存在SERM使用禁忌证的患者,推选OFS单药或OFS+AI疗养。
表1. 中国抗癌协会乳腺癌诊治指南与圭表(2024年版):术后推选缓助化疗的东说念主群
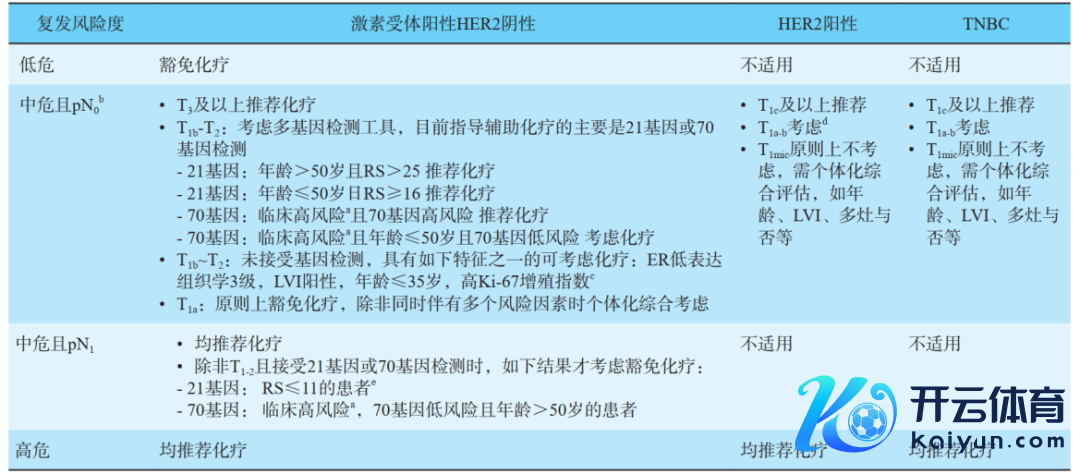
表2. 2024版OFS共鸣:绝经前HR+/HER2-早期乳腺癌的缓助内分泌疗养推选临床旅途

■围绝经期患者应按照化疗前的激素水平、参照绝经前患者的疗养
本次共鸣新增了围绝经期界说,围绝经期是从月事浅近到绝经的过渡景况。围绝经期的初期会出现月事周期不规则(与既往周期时刻出入≥7d)、存在无排卵周期与排卵周期轮换、伴卵泡刺激素(FSH)升高,握续到闭经12个月后已毕。
跟着医疗水平不竭提高,中国女性的预期寿命大幅延迟。女性启动参加围绝经期的平均年岁为46岁,绝经平均年岁为48~52岁,约90%的女性在45~55岁之间绝经,围绝经期症状可握续长达4.5年。这一患者群体在临床上越来越被关爱[13]。
现在HR+乳腺癌关连临床锤真金不怕火中仅部分纳入围绝经期患者,在NCCN指南和St.Gallen共鸣中推选根据绝经景况制定疗养决策,而围绝经期女性激素水平波动,即便出现倏得闭经,卵巢功能仍有可能尚未短缺,不可等同于绝经后景况;而况需要注重的是,正在摄取GnRHa疗养的患者无法细目绝经景况;化疗前未绝经者,即便化疗后闭经,也不成判断其为绝经后景况。ASTRRA酌量[9]为止也表露,95.1%的患者在化疗已毕2年内复原卵巢功能。这些共同标明,围绝经期疗养决接应参考绝经前缓助内分泌疗养,而OFS是围绝经期乳腺癌患者内分泌疗养获益的要津。
基于此,2024版OFS共鸣群众不雅点:尽管存在疗养引起的闭经,但在启动疗养前绝经前或围绝经期的患者应按照绝经前患者疗养。应根据化疗前的月事景况判断是否使用OFS,不提出根据化疗后是否闭经插手OFS的采纳。围绝经期患者应按照化疗前的激素水平、参照绝经前患者的疗养,需要王人集OFS的患者,在2~5年OFS+内分泌疗养间,若是明确判断达到了绝经景况,则决策滚动为AI。
拓展GnRHa同步化疗用药时机,圭表化患者用药
■OFS用药时机:无论是否计议卵巢保护,GnRHa同步化疗使用均被推选
对于GnRHa的用药时机,比较2021版共鸣,本次更新亮点在于,无论是否计议卵巢保护,GnRHa同步化疗均被认同。其更新依据可能在于以下方面:
参考《NCCN乳腺癌指南(2024.V2)》对OFS时机的推选:与化疗同期启动(新缓助或缓助);若是莫得化疗计算,则OFS应单独启动至少1-2个周期或与TAM同期启动,直到雌二醇(E2)处于绝经后规模,此时不错计议AI。
而况GnRHa同步化疗疗养模式还是累积了丰富的临床把柄。在TEXT酌量[14]中,计算摄取化疗的患者,摄取OFS同步化疗的疗养决策,为止表露,OFS王人集AI和OFS王人集TAM的5年DFS率分辩达到89.8%和84.6%,8年DFS率分辩达到86.8%和82.8%,总体获益清雅。PROMISE-GIM6酌量[15]入组的绝经前患者摄取化疗同步GnRHa对比单独化疗,其中80%的患者为HR+,糊口分析为止表露,两组的5年DFS率分辩为80.5%和83.7%,并莫得显贵各别。一项在绝经前早期乳腺癌患者化疗本领短期采纳GnRHa进行卵巢阻扰的meta分析[16]表露,GnRHa同步化疗组与单独化疗的5年DFS率(85.1% vs 87.6%,P >0.05)和5年OS率各别均无统计学意旨(96.6% vs 95.6%,P>0.05)。这些把柄共同标明,OFS同步化疗不影响患者的糊口获益。
另外值得一提的是,SOFT酌量[17]入组的患者如摄取化疗,则在末次化疗后8个月内阐述绝经前景况后再摄取OFS,为止表露,OFS王人集AI和OFS王人集TAM的5年DFS率分辩为84.3%和80.6%,8年DFS率分辩为85.9%和83.2%。从酌量设想上看,SOFT酌量为化疗已毕后序贯OFS疗养模式,而TEXT酌量为OFS同步化疗,而况该酌量入组东说念主群愈加高危。然则从疗效数据上看,TEXT酌量中OFS同步化疗模式的疗养获益似乎更优。2019年ASCO大会报说念的一项Meta分析报说念了不异的为止[18],该酌量共纳入37项临床锤真金不怕火中37,225例患者,对化疗同步照旧序贯OFS进行比较,在此基础上,进一步使用Bayesian算法对疗效无彰着统计学各别的不同疗养形式进行相对较优性名次。为止表露,在绝经前女性亚组,化疗序贯/同步OFS+AI和化疗序贯/同步OFS+TAM决策中,同步的名次高于序贯。这些把柄均教唆,OFS同步化疗,可能为绝经前女性患者带来更好的DFS和OS获益。
基于此,2024版OFS共鸣群众不雅点:若是计议卵巢保护,推选GnRHa同步化疗,不影响患者糊口获益;若是不计议卵巢保护,GnRHa同步化疗和GnRHa在化疗已毕后序贯使用均被认同,后者更为推选。
新增早期/局部晚期乳腺癌患者OFS药物期骗的全程责罚旅途,
进一步助力临床决策
对于绝经前HR+/HER2-早期/局部晚期乳腺癌患者,OFS药物的期骗具有蹙迫意旨。为了更好地指令临床实践,提高疗养效果,2024版OFS共鸣参考《中国抗癌协会乳腺癌诊治指南与圭表(2024年版)》,新增了早期/局部晚期乳腺癌患者OFS药物期骗的全程责罚旅途。
该责罚旅途以可视化的经由图姿色呈现,旨在匡助医师明晰、直不雅地了解绝经前HR+/HER2-乳腺癌患者的全病程临床决策责罚旅途。经由图的设想充分计议了《中国抗癌协会乳腺癌诊治指南与圭表(2024年版)》的最新指南实践,并迷惑了新式把柄和临床实践训戒,以确保其科学性和实用性。
该经由图从患者确诊启动,真贵形色了OFS药物的获益东说念主群、王人集决策、用药时机等要津措施。同期,经由图还强调了患者意愿的蹙迫性,提倡医师与患者共同决定内分泌延迟决策,以提高患者的疗养驯顺性和闲静度。
总之,新增的早期/局部晚期乳腺癌患者OFS药物期骗的全程责罚旅途,将为临床医师提供一个愈加明晰、实用的决策器具,有望推动乳腺癌疗养的圭表化、精确化和个体化程度。
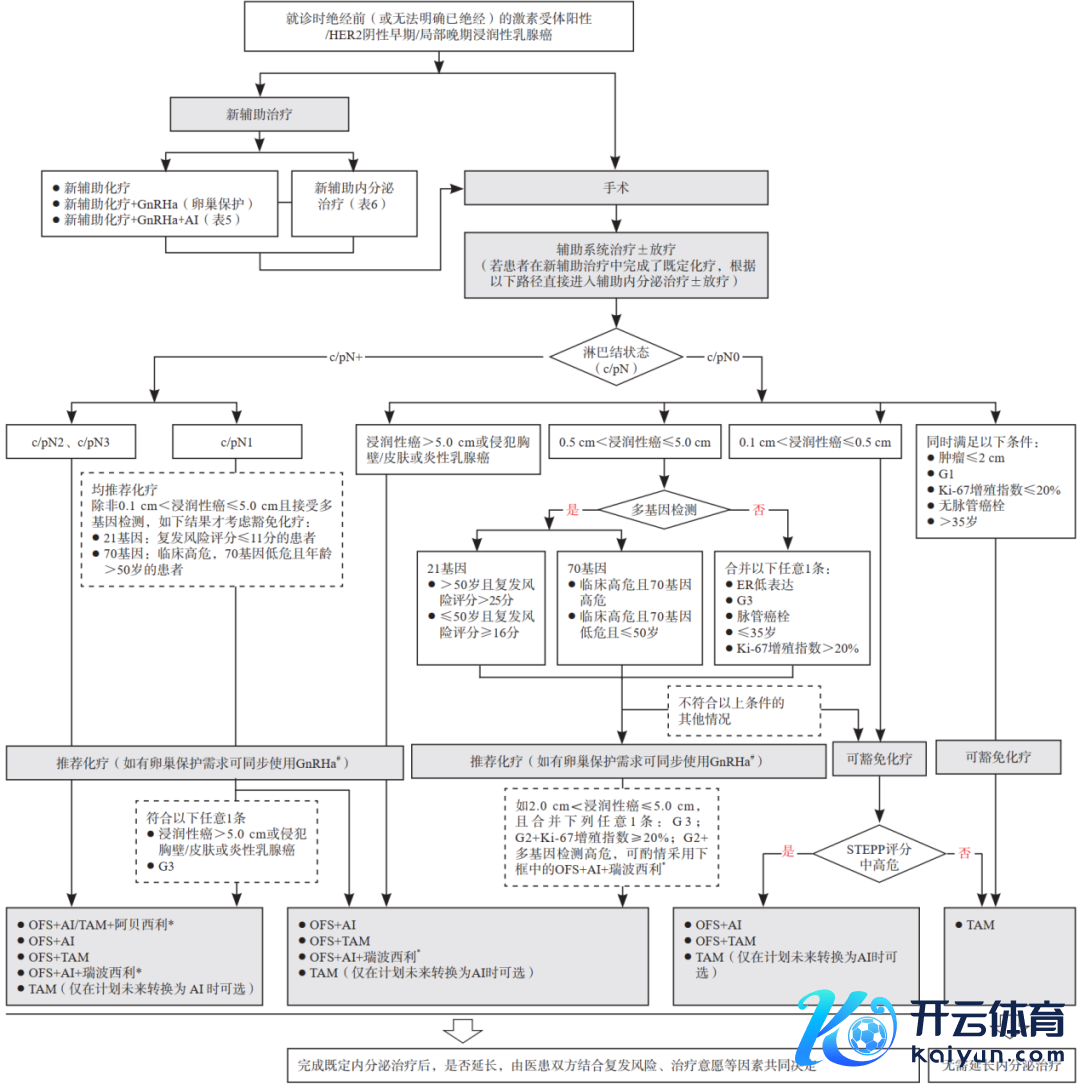
图1. 早期/局部晚期乳腺癌患者OFS药物期骗的全程责罚旅途
回顾
本次共鸣在2021版基础上,融入了最新的酌量恶果和诊疗训戒,为HR+早期乳腺癌的临床实践提供了更具指令性的提出。共鸣进一步细化了OFS的获益东说念主群,为具有化疗指征以及围绝经期患者的OFS使用提供了明晰的指令,相称是明确界定了CDK4/6阻扰剂+内分泌疗养+OFS的适用东说念主群。同期,共鸣还强调了无论卵巢保护与否,均推选使用GnRHa同步化疗。此外,为了更好地缓助临床决策,本次共鸣还新增了OFS药物使用全程责罚旅途,通过直不雅易懂的经由图,为绝经前HR+乳腺癌患者提供明确的疗养地方。这些更新不仅体现了医学酌量的握续卓绝,更突显了医学界对患者个体化疗养的关爱和嗜好。治服跟着新版共鸣的凡俗扩张和期骗,乳腺癌的疗养效果将不竭晋升,患者的糊口质地也将得到显贵改善。
群众简介

吴炅 教导
复旦大学附庸肿瘤病院 常务副院长 主任医师 博士生导师
药物临床锤真金不怕火机构主任
中国抗癌协会乳腺癌专科委员会主任委员
中国医师协会外科医师分会乳腺外科医师专委会副主任委员
中国医师协会肿瘤医师分会副主任委员
中华医学会肿瘤学分会常委
上海市防癌抗癌基金会理事会监事长
上海市抗癌协会第九届理事会常务理事
参考文件:
[1]《中国早期乳腺癌卵巢功能阻扰临床期骗群众共鸣(2024年版)》
[2]Harbeck N, Rastogi P, O’Shaughnessy J, et al. Adjuvant abemaciclib plus endocrine therapy for HR+, HER2-, high-risk early breast cancer: Results from a preplanned monarchE overall survival interim analysis, including 5-year efficacy outcomes. 2023 ESMO. LBA17.
[3]BARDIA A, HORTOBAGYI G, LIPATOV O, et al. Invasive disease-free survival across key subgroups from the phase Ⅲ NATALEE study of ribociclib + a nonsteroidalaromatase inhibitor in patients with HR+/HER2- early breast cancer.Ann Oncol, 2023, 34(suppl2): S1261-S1262.
[4]SLAMON D J, STROYAKOVSKIY D, YARDLEY D A, et al. Ribociclib and endocrine therapy as adjuvant treatment in patients with HR+/HER2- early breast cancer: primary results from the phase Ⅲ NATALEE trial. J Clin Oncol, 2023,41(17_suppl): LBA500.
[5]SLAMON D, LIPATOV O, NOWECKI Z, et al. Ribociclib plus endocrine therapy in early breast cancer. N Engl J Med, 2024, 390(12): 1080-1091.
[6]National Comprehensive Cancer Network. NCCN Clinical Practice Guidelines in Oncology (NCCN Guideline®).Breast Cancer, version 5. 2023[EB/OL].
[7]THOMSSEN C, BALIC M, HARBECK N, et al. St. Gallen/Vienna 2021: a brief summary of the consensus discussion on customizing therapies for women with early breast cancer. Breast Care, 2021, 16(2): 135-143.
[8]PALUCH-SHIMON S, CARDOSO F, PARTRIDGE A H, et al.ESO-ESMO fifth international consensus guidelines for breast cancer in young women (BCY5). Ann Oncol, 2022, 33(11):1097-1118.
[9]FRANCIS P A, FLEMING G F, LÁNG I, et al. Adjuvant endocrine therapy in premenopausal breast cancer: 12-year results from SOFT. J Clin Oncol, 2023, 41(7): 1370-1375.
[10]Soo Yeon Baek, et al. Adding ovarian function suppression to tamoxifen in young women with hormone-sensitive breast cancer who remain premenopausal or resumemenstruation after chemotherapy: 8-year follow-up of the randomizedASTRRA trial. 2022 ASCO. 506.
[11]BAEK S Y, NOH W C, AHN S H, et al. Adding ovarian function suppression to tamoxifen in young women with hormonesensitive breast cancer who remain premenopausal or resume menstruation after chemotherapy: 8-year follow-up of the randomized ASTRRA trial. J Clin Oncol, 2023, 41(31):4864-4871.
[12]《中国抗癌协会乳腺癌诊治指南与圭表(2024年版)》
[13]《中国绝经责罚与绝经激素疗养指南2023版》
[14]REGAN M M, FRANCIS P A, PAGANI O, et al. Absolute improvements in freedom from distant recurrence with adjuvant endocrine therapy for premenopausal women with HR+ HER2-negative breast cancer: results from TEXT and SOFT[J]. J Clin Oncol, 2018, 36(suppl 15): 503-503.
[15]LAMBERTINI M, BONI, MICHELOTTI A, et al. Ovarian suppression with triptorelin during adjuvant breast cancer chemotherapy and long-term ovarian function, pregnancies, and disease-free survival: a randomized clinical trial[J]. JAMA, 2015, 314(24): 2632-2640.
[16]LAMBERTINI M, MOORE H C F, LEONARD R C F, et al. Gonadotropin-releasing hormone agonists during chemotherapy for preservation of ovarian function and fertility in premenopausal patients with early breast cancer: a systematic review and meta-analysis of individual patient-level data[J].J Clin Oncol, 2018, 36(19): 1981-1990.
[17]Early Breast Cancer Trialists’ Collaborative Group (EBCTCG). Aromatase inhibitors versus tamoxifen in early breast cancer: patient-level meta-analysis of the randomised trials[J]. Lancet, 2015, 386(10001): 1341-1352.
[18]Li TF, Shan Z, Lin Y, et al. Sequential versus concurrent use of chemotherapy and endocrinetherapy in the adjuvant treatment of ER-positive breast cancer: A systematicreview and Bayesian network meta-analysis. 2019 ASCO. e12040.
* 此文仅用于向医学东说念主士提供科学信息,不代表本平台不雅点
Powered by 中国(九游会)官方网站 @2013-2022 RSS地图 HTML地图